L’hamstring syndrome
Introduzione
L’hamstring syndrome (HS) venne descritta per la prima volta da Puranen ed Horawa nel 1988 ed inquadrata nell’ambito di una tendinopatia inserzionale prossimale degli hamstring. Classicamente con il termine di HS s’intende appunto una tendinopatia inserzionale prossimale degli hamstring in cui la formazione di un tessuto fibrotico, associato ad una pregressa lesione della componente tendinea od una sua degenerazione che comporti un aumento del calibro del tendine stesso, causi una compressione a livello dell’adiacente nervo sciatico (Puranen e Horawa, 1988, Sherry 2012). Molto spesso quindi la HS rappresenta un esito di lesione parziale della UMT prossimale degli hamstring (Puranen e Horawa, 1988; Askling e coll., 2006; Lempainen e coll., 2009; Saikku e coll., 2010; Cacchio e coll., 2011). In letteratura la HS si ritrova associata a pregressi eventi lesivi indiretti della UMT degli hamstring in una percentuale compresa tra il 76 ed il 19% dei casi (Agre, 1985; Hartig, 1999; Fredericson e coll., 2005; Clark, 2008; Young e coll., 2008; Lempainen e coll., 2009; Benazzo e coll., 2013).
Anche se inizialmente l’HS è stata descritta in una popolazione di sprinter (Puranen e Horawa, 1988), le evidenze più recenti suggeriscono di come sia invece di maggior riscontro nei mezzofondisti, nei calciatori e negli sciatori di fondo (Puranen e Horawa, 1988; Fredericson e coll., 2005; Lempainen e coll., 2009; Cacchio e coll., 2011). L’età di maggior frequenza è compresa tra i 29 ed i 37 anni (Young e coll., 2008; Lempainen e coll., 2009; Zissen e coll., 2010).
La diagnosi clinica
La maggior parte dei pazienti affetta da HS lamenta un sintomatologia algica elettiva, di intensità variabile, alla palpazione a livello dell’inserzione prossimale degli hamstring (Puranen e Horawa, 1988; Fredericson e coll., 2005; Young e coll., 2008; Lempainen e coll., 2009; Cacchio e coll., 2011), mentre i test manuali a carico della muscolatura flessoria e di quella glutea possono anche rientrare in un range di normalità (Agre, 1985; Sherry, 2012). Anche i test neurologici periferici generalmente appaiono nella norma (Agre, 1985; Lempainen e coll., 2009). Generalmente il paziente riferisce una sensazione di disconfort a livello inserzionale prossimale nel corso dei test di flessibilità, che possono peraltro non mostrare dei deficit significativi (Puranen e Horawa, 1988; Lempainen e coll., 2009). Durante l’esecuzione dell’ hamstring-stretch test (HST) (figura 1) si ha positività nel caso di evocazione di sintomatologia algica elettiva a livello dell’inserzione prossimale degli hamstring (Cacchio e coll., 2011). Test simili all’HST, e che si prefiggono la stessa finalità, sono il Puranen-Orawa test (figura 2) ed il bent-knee stretch test (figura 3). Dal momento che l’HS spesso comporta un ipotonotrofia dei muscoli abduttori della coscia (White, 2010), non è infrequente che il test di Trendelenburg sia positivo sul lato affetto (Fredericson e coll., 2000). In funzione del grado compressione a livello del nervo sciatico i pazienti possono mostrare una sintomatologia radicolare più o meno evidente (Lempainen e coll., 2009; Cacchio e coll., 2010). In genere l’HS non impedisce totalmente l’attività di corsa ma, in ogni caso, la limita fortemente, ed in genere la sintomatologia algica è esacerbata dalla corsa in salita, in discesa e durante lo sprint , rimando al contrario piuttosto contenuta durante la corsa a bassa velocità effettuata su terreno pianeggiante.
Infine, è importante ricordare che tipicamente il paziente affetto da HS riferisce l’insorgenza di sintomatologia algica elettiva a livello dell’inserzione prossimale dei muscoli flessori della coscia nel mantenimento della posizione seduta soprattutto su superfici rigide (Fredericson e coll., 2005).
L’imaging
Nel caso di HS l’imaging di prima scelta è rappresentata dalla RM attraverso la quale si possono evidenziare (Fredericson e coll., 2005; Lempainen e coll., 2009; White, 2010; Zissen e coll., 2010; Cacchio e coll., 2011; ):
- Un inspessimento del calibro tendineo;
- Una lesione parziale del tendine;
- Una eterogeneità del segnale intratendineo;
- Un bone marrow edema a livello della tuberosità ischiatica;
- Identificare una compressione del nervo sciatico nel suo decorso prossimale.
Generalmente si evidenzia un incremento di segnale nelle sequenze pesate in T1, senza invece che si riscontrino significative anormalità di segnale, a parte la possibile presenza di bone marrow edema, nelle sequenze pesate in T2. Le lesioni focali parziali della struttura tendinea appariranno invece come un incremento di segnale in entrambe le sequenze (Fredericson e coll., 2005).
Ultimamente nell’ambito della diagnosi per imaging della HS , grazie alla sua facile reperibilità ed alla sua relativa economicità, si sta diffondendo l’uso dell’esame ecotomografico (US) (Zissen, 2010; Sherry, 2012). Tuttavia l’US, oltre a rendere impossibile l’identificazione della presenza o meno di un possibile bone marrow edema, presenta il non sottovalutabile limite di una scarsa sensitività (Zissen, 2010; Sherry, 2012).
La diagnosi differenziale
Nell’ambito della diagnosi di HS la diagnosi differenziale deve considerare (Brandser e coll., 1995; Lempainen e coll., 2009):
- Possibili lesioni indirette degli hamstring;
- Sindrome del piriforme;
- Borsite ischiatica;
- Lombosciatalgia;
- Sindrome compartimentale cronica della coscia;
- Ematomi profondi;
- Tumori dei tessuti molli.
Il trattamento conservativo
Il trattamento conservativo rappresenta la prima scelta terapeutica nell’ambito dell’HS. Un corretto trattamento conservativo dovrebbe considerare i seguenti punti:
- Un eventuale riallineamento pelvico
- Mobilizzazione dei tessuti molli;
- Stretching attivo e passivo sotto diverse forme e modalità della muscolatura degli hamstring;
- Condizionamento eccentrico della muscolatura degli hamstring;
- Stabilizzazione del Core.
La Extra Wave Schock Terapy ha mostrato una limitata evidenza anche se in un recente studio (Cacchio e coll., 2011) ne avrebbero dimostrato i possibili benefici. Pertanto, nonostante questi risultati incoraggianti, si renderebbero necessari ulteriori studi che possano confermarne la validità e standardizzarne i protocolli.
L’iniezione locale di corticosteroidi avrebbe un outcome positivo in poco più del 20% dei casi e la risoluzione della sintomatologia si mostrerebbe in ogni caso di breve durata e comunque non maggiore di 6 mesi (Zissen, 2010). Le terapie rigenerative, sostanzialmente basate sull’utilizzo di platelet-rich plasma, non mostrano ad oggi, in ambito tendineo, una sufficiente evidenza (Bisciotti, 2013).
Il trattamento chirurgico
Nel caso di fallimento del trattamento conservativo l’HS spesso richiede un approccio di tipo chirurgico (Young e coll., 2008; Lempainen e coll., 2009) . Generalmente viene effettuata una tenotomia trasversale del tendine del semimembranoso eseguita a 3-4 centimetri distalmente rispetto alla sua origine, seguita dalla sua successiva saturazione a livello del bicipite femorale (Orawa, 1997; Young e coll., 2008; Lempainen e coll., 2009). Alcuni Autori (Orawa, 1997) accoppiano a tale tipo di tecnica chirurgica anche la neurolisi del tendine interessato. Altri Autori (Benazzo e coll., 2013) preferiscono effettuare una tenotomia trasversale parziale del tendine inspessito e avvolto dalla guaina fibrosa, seguita da un sistematico release del nervo sciatico effettuato a partire dalla tuberosità ischiatica e protratto distalmente per una lunghezza di circa 10 centimetri. Il periodo riabilitativo dopo trattamento chirurgico ha una durata compresa tra i 60 ed i 90 giorni ed i follow-up a lungo termine (da 2 a 10 anni) che riportano risultati definiti come “eccellenti” e “buoni”sono compresi tra il 77 e l’88% dei casi considerati (Orawa, 1997; Young e coll., 2008; Lempainen e coll., 2009; Benazzo e coll., 2013).
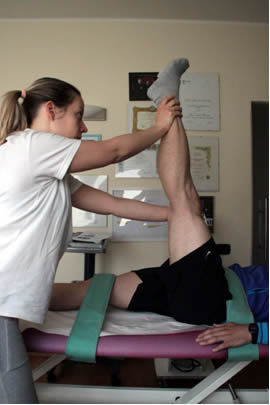
Figura 1:
l’esecuzione dell’ hamstring-stretch test prevede che l’operatore effettui una rapida flessione dell’anca immediatamente seguita da un’altrettanto rapida estensione della gamba sulla coscia. Il test risulta positivo se evoca una sintomatologia algica elettiva a livello dell’inserzione prossimale degli hamstring.

Figura 2:
nel Puranen-Orawa test il paziente effettua uno stretching attivo in ortostatismo della muscolatura degli hamstring. Anche in questo caso il test risulta positivo se provoca dolore elettivo al livello dell’inserzione prossimale dei flessori.

Figura 3:
nel bent-knee stretch test il soggetto effettua con l’ausilio di una fascia o di una corda uno stretching attivo della muscolatura flessoria dalla posizione supina. Il test è positivo se evoca dolore elettivo a livello dell’inserzione prossimale degli hamstring.
Agre JC. Hamstring injuries. Proposed aetiological factors, prevention, and treatment. Sports Med. 1985; 2(1):21–33.
Askling CM, Tengvar M, Saartok T, Thorstensson A. Acute first-time hamstring strains during high-speed running: a longitudinal study including clinical and magnetic resonance imaging findings. Am J Sports Med. 2006;35(2):197-206.
Benazzo F., Zanon MG., Indino C., Pelillo F. Surgical management of chronic proximal hamstring tendinopathy in athletes: a 2 to 11 years of follow-up. J Orthopaed Traumatol (2013) 14:83–89.
Bisciotti GN. I tendini. Biologia, patologia, aspetti clinici. Volume 1 (Anatomia ed aspetti generali). Calzetti e Mariucci Eds. Perugia, 2013.
Brandser E, El-Khoury G, Kathol M, Callaghan J, Tearse D Hamstring injuries: radiographic, conventional tomographic, CT, and MR imaging characteristics. Semin Musculoskel Radiol 1995;197:257-62.
Cacchio A, Rompe JD, Furia JP, Susi P, Santilli V, De Paulis F. Shockwave therapy for the treatment of chronic proximal hamstring tendinopathy in professional athletes. Am J Sports Med. 2011;39(1):146-153.
Clark RA. Hamstring injuries: risk assessment and injury prevention. Ann Acad Med Singapore 2008;37(4):341-6.
Fredericson M, Cookingham CL, Chaudhari AM, Dowdell BC, Oestreicher N, Sahrmann SA. Hip abductor weakness in distance runners with illiotibial band syndrome. Clin J sport Med 2000;10(3):169-75.
Fredericson M, Moore W, Guillet M, Beaulieu C. High hamstring tendinopathy in runners: meeting the challenges of diagnosis, treatment, and rehabilitation. Phys Sports Med. 2005;33(5):32-43.
Hartig D. Increasing hamstring flexibility decreases lower extremity overuse injuries in military basic trainees. Am J Sports Med 1999;27(2):173-6.
Lempainen L, Sarimo J, Mattila K, Vaittinen S, Orava S. Proximal hamstring tendinopathy: results of surgical management and histopathologic findings. Am J Sports Med. 2009;37(4):727-734.
Orava S Hamstring syndrome. Oper Tech Sports Med. 1997; 5:143–149.
Puranen J, Orava S (1988) The hamstring syndrome. A new diagnosis of gluteal sciatic pain. Am J Sports Med 16(5):517–521.
Saikku K, Vasenius J, Saar P. Entrapment of the proximal sciatic nerve by the hamstring tendons. Acta Orthop Belg. 2010;76(3):321-324.
Sherry, MA Evaluation and Treatment of Acute Hamstring Strains and Related Injuries. Sports Physical Therapy. 2012; 4(2): 107-114.
Young IJ, van Riet RP, Bell SN. Surgical release for proximal hamstring syndrome. Am J Sports Med. 2008; 36(12):2372–2378.
Zissen MH, Wallace G, Stevens KJ, Fredericson M, Beaulieu CF. High hamstring tendinopathy: MRI and ultrasound imaging and therapeutic efficacy of percutaneous corticosteroid injection. AJR Am J Roentgenol. 2010;195(4):993-998.
